Papildus tehnoloģijām, glikozīdu sintēze vienmēr ir interesējusi zinātni, jo tā ir ļoti izplatīta reakcija dabā. Šmita, Tošimas un Tatsutas nesenajos rakstos, kā arī daudzās tajos citētajās atsaucēs ir sniegts komentārs par plašu sintētisko potenciālu klāstu.
Glikozīdu sintēzē daudzcukuru komponenti tiek apvienoti ar nukleofiliem, piemēram, spirtiem, ogļhidrātiem vai olbaltumvielām. Ja nepieciešama selektīva reakcija ar vienu no ogļhidrāta hidroksilgrupām, pirmajā posmā ir jāaizsargā visas pārējās funkcijas. Principā fermentatīvie vai mikrobiālie procesi, pateicoties to selektivitātei, var aizstāt sarežģītus ķīmiskās aizsardzības un aizsardzības noņemšanas soļus, lai selektīvi atbrīvotos no glikozīdiem noteiktos reģionos. Tomēr alkilglikozīdu ilgās vēstures dēļ fermentu pielietojums glikozīdu sintēzē nav plaši pētīts un pielietots.
Piemērotu enzīmu sistēmu jaudas un augsto ražošanas izmaksu dēļ alkilpoliglikozīdu enzīmu sintēze nav gatava modernizācijai rūpnieciskā līmenī, un priekšroka tiek dota ķīmiskām metodēm.
1870. gadā Makolijs ziņoja par “acetohlorhidrozes” (1, 2. attēls) sintēzi, dekstrozi (glikozi) reaģējot ar acetilhlorīdu, kas galu galā noveda pie glikozīdu sintēzes ceļu vēstures.
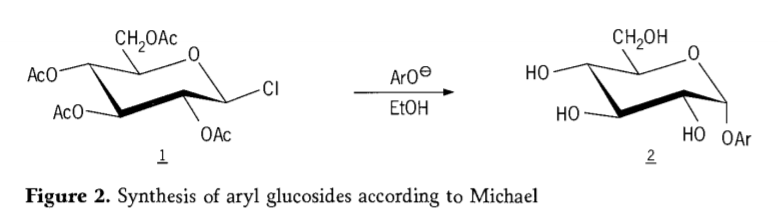
Vēlāk tika atklāts, ka tetra-0-acetil-glikopiranozilhalogenīdi (acetohalogēnglikozes) ir noderīgi starpprodukti tīru alkilglikozīdu stereoselektīvai sintēzei. 1879. gadā Artūram Maiklam izdevās no Kollija starpproduktiem un fenolātiem sagatavot noteiktus, kristalizējamus arilglikozīdus. (Aro-, 2. attēls).
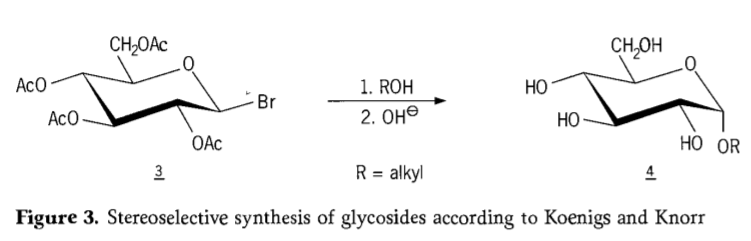
1901. gadā Maikla sintēze plašā ogļhidrātu un hidroksilslāņaglikonu klāstā, kad V. Kēnigss un E. Nors ieviesa savu uzlaboto stereoselektīvo glikozilēšanas procesu (3. attēls), ļāva iegūt plašu ogļhidrātu un hidroksilslāņa aglikonu klāstu. Reakcija ietver SN2 aizvietošanu pie anomēriskā oglekļa un norit stereoselektīvi ar konfigurācijas inversiju, piemēram, iegūstot α-glikozīdu 4 no aceobromglikozes starpprodukta 3 β-anomēra. Kēnigsa-Nora sintēze notiek sudraba vai dzīvsudraba promotoru klātbūtnē.
1893. gadā Emīls Fišers ierosināja principiāli atšķirīgu pieeju alkilglikozīdu sintēzei. Šis process tagad ir labi pazīstams kā "Fišera glikozidēšana" un ietver skābes katalizētu glikožu reakciju ar spirtiem. Jebkurā vēsturiskā aprakstā tomēr jāiekļauj arī A. Gotjē pirmais zināmais mēģinājums 1874. gadā pārvērst dekstrozi ar bezūdens etanolu sālsskābes klātbūtnē. Maldinošas elementanalīzes dēļ Gotjē uzskatīja, ka ir ieguvis "diglikozi". Fišers vēlāk pierādīja, ka Gotjē "diglikoze" patiesībā galvenokārt bija etilglikozīds (4. attēls).
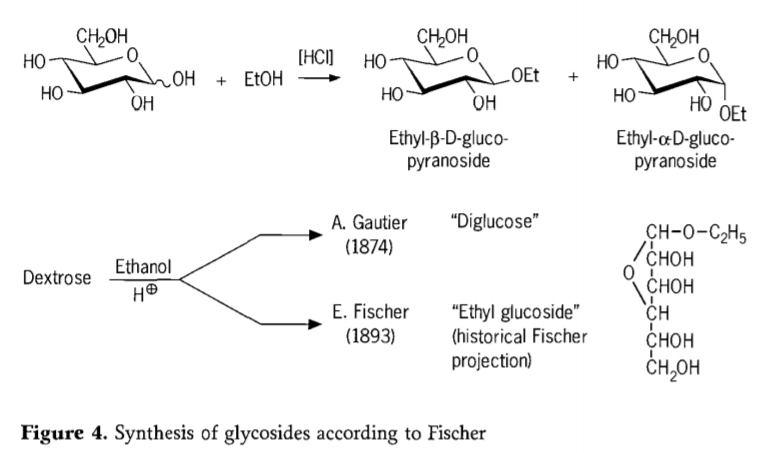
Fišers pareizi definēja etilglikozīda struktūru, kā redzams no vēsturiski piedāvātās furanozīda formulas. Faktiski Fišera glikozilācijas produkti ir sarežģīti, pārsvarā līdzsvara stāvoklī esoši α/β-anomēru un piranozīda/furanozīda izomēru maisījumi, kas satur arī nejauši saistītus glikozīdu oligomērus.
Attiecīgi atsevišķas molekulu sugas nav viegli izolēt no Fišera reakcijas maisījumiem, kas agrāk ir bijusi nopietna problēma. Pēc šīs sintēzes metodes uzlabošanas Fišers vēlāk savos pētījumos izmantoja Kēnigsa-Knora sintēzi. Izmantojot šo procesu, E. Fišers un B. Helferihs bija pirmie, kas 1911. gadā ziņoja par garas ķēdes alkilglikozīda, kam piemīt virsmaktīvās vielas īpašības, sintēzi.
Jau 1893. gadā Fišers pareizi pamanīja alkilglikozīdu būtiskās īpašības, piemēram, to augsto stabilitāti pret oksidēšanos un hidrolīzi, īpaši stipri sārmainā vidē. Abas īpašības ir vērtīgas alkilpoliglikozīdiem virsmaktīvo vielu pielietojumos.
Pētījumi, kas saistīti ar glikozidācijas reakciju, joprojām turpinās, un nesenā pagātnē ir izstrādāti vairāki interesanti glikozīdu iegūšanas ceļi. Dažas no glikozīdu sintēzes procedūrām ir apkopotas 5. attēlā.
Kopumā ķīmiskās glikozilēšanas procesus var iedalīt procesos, kas noved pie sarežģīta oligomēru līdzsvara skābes katalizētā glikozilu apmaiņā.
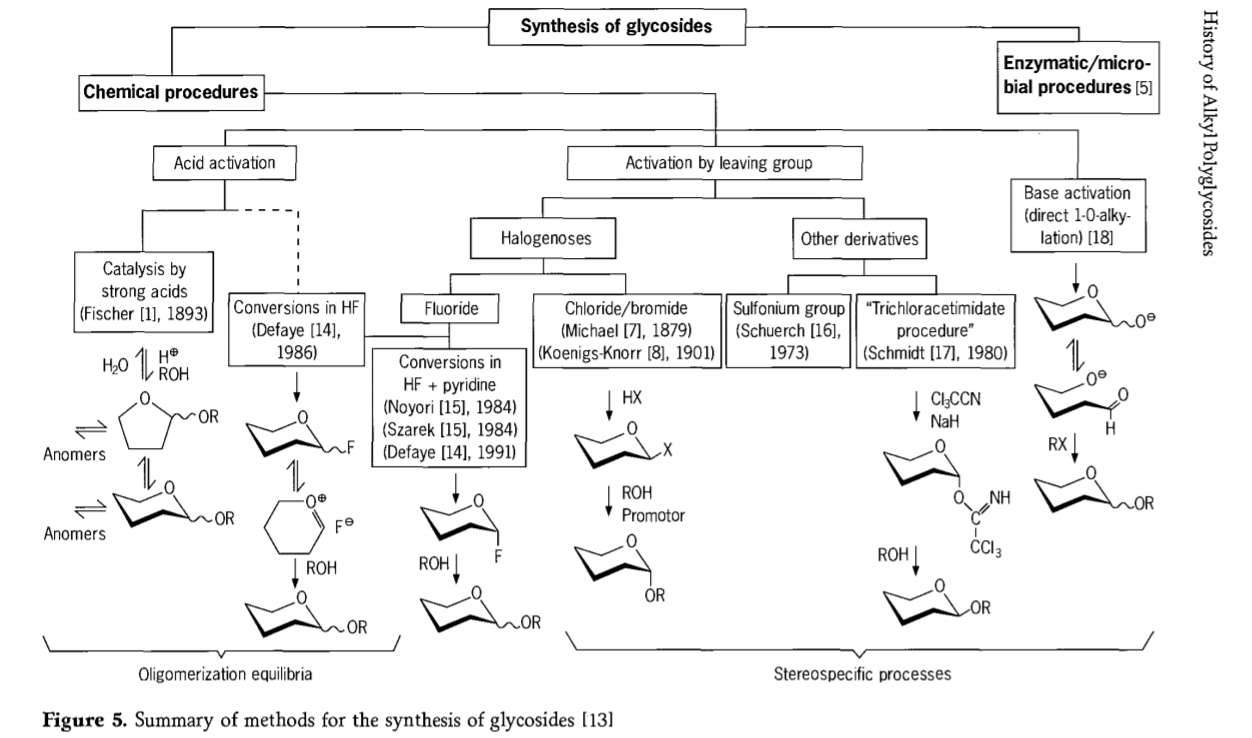
Reakcijas uz atbilstoši aktivizētiem ogļhidrātu substrātiem (Fišera glikozīdiskās reakcijas un ūdeņraža fluorīda (HF) reakcijas ar neaizsargātām ogļhidrātu molekulām) un kinētikas kontrolētas, neatgriezeniskas un galvenokārt stereotaksiskas aizvietošanas reakcijas. Otra veida procedūra var izraisīt atsevišķu sugu veidošanos, nevis sarežģītus reakciju maisījumus, īpaši, ja to kombinē ar saglabāšanas grupu metodēm. Ogļhidrāti var atstāt grupas uz ektopiskā oglekļa, piemēram, halogēna atomus, sulfonilu grupas vai trihloracetimidāta grupas, vai arī tos var aktivizēt ar bāzēm pirms pārvēršanas triflāta esteros.
Konkrētajā glikozilēšanas gadījumā ūdeņraža fluorīdā vai ūdeņraža fluorīda un piridīna maisījumos (piridīnija poli[ūdeņraža fluorīds]), glikozilfluorīdi veidojas in situ un, piemēram, ar spirtiem, tiek vienmērīgi pārveidoti par glikozīdiem. Ir pierādīts, ka ūdeņraža fluorīds ir spēcīgi aktivizējoša, nenoārdoša reakcijas vide; tiek novērota līdzsvara autokondensācija (oligomerizācija) līdzīgi Fišera procesam, lai gan reakcijas mehānisms, iespējams, atšķiras.
Ķīmiski tīri alkilglikozīdi ir piemēroti tikai ļoti īpašiem pielietojumiem. Piemēram, alkilglikozīdi ir veiksmīgi izmantoti bioķīmiskajos pētījumos membrānu olbaltumvielu kristalizācijai, piemēram, porīna un bakteriorodopsīna trīsdimensiju kristalizācijai oktil-β-D-glikopiranozīda klātbūtnē (turpmākie eksperimenti, kas balstīti uz šo darbu, noveda pie Nobela prēmijas ķīmijā Deizenhoferam, Hūberam un Mišelam 1988. gadā).
Alkilpoliglikozīdu izstrādes gaitā laboratorijas mērogā ir izmantotas stereoselektīvās metodes, lai sintezētu dažādas modeļvielas un pētītu to fizikāli ķīmiskās īpašības. To sarežģītības, starpproduktu nestabilitātes un procesa atkritumu daudzuma un kritiskā rakstura dēļ Kēnigsa-Knora tipa sintēzes un citas aizsarggrupu metodes radītu ievērojamas tehniskas un ekonomiskas problēmas. Fišera tipa procesi ir salīdzinoši mazāk sarežģīti un vieglāk īstenojami komerciālā mērogā, un attiecīgi ir vēlamā metode alkilpoliglikozīdu ražošanai plašā mērogā.
Publicēšanas laiks: 2020. gada 12. septembris





